Práctica. Física y Química. N15. B. Compuestos binarios del hidrógeno. 2013
Contents |
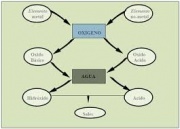
Introducción
El hidrógeno es uno de los pocos elementos químicos que se combina con casi todos los demás. Los compuestos resultantes de la unión del hidrógeno y otro elemento se denomina hidruro, con la excepción del flúor, cloro, bromo, yodo, azufre, selenio, teluro y el oxígeno (ver punto Compuestos especiales )
Fórmula general
Los hidruros son compuestos binarios formados por hidrógeno y otro elemento. En la fórmula el hidrógeno actúa con valencia -1, en las fórmulas, el elemento químico se pone delante del hidrógeno indicando la valencia de cada uno poniéndolo en el elemento contrario.
XHnúmero de oxidación del elementoXExiste una excepción, que sucede cuando el hidrógeno se combina con: cloro, bromo, yodo, azufre, selenio, flúor y teluro Hxnúmero de oxidación del elemento X
Nomenclatura con números de oxidación
La nomenclatura con prefijos multiplicadores se utilizan los prefijos numerales griegos para numerar los átomos de hidrógeno.
La nomenclatura con números de oxidación se indica el número de oxidación del elemento unido al hidrógeno mediante números romanos entre paréntesis, aunque, a veces no es necesario ponerlo.
Ejemplos BeH2(di)hidruro de berilio o hidruro de berilio
AlH3(tri)hidruro de aluminio o hidruro de aluminio
BaH2(di)hidruro de bario o hidruro de bario
CuH(mono)hidruro de cobre o Hidruro de cobre(I)
CuH2dihidruro de cobre o Hidruro de cobre(II)
FeH3trihidruro de hierro o Hidruro de hierro(III)
Algunos compuestos binarios del hidrogeno reciben nombres comunes como:
NH3 Amoniaco, H2O Agua, CH4 Metano
Compuestos especiales
Con algunos compuestos como el flúor, el cloro, el bromo, el yodo, el azufre, el selenio y el teluro; el hidrógeno actúa con numero de oxidación +1, y el átomo lo hace con su número de oxidación negativo.La fórmula general de estos compuestos, se escribe, en primer lugar, el símbolo del hidrógeno con el número de oxidación del elemento X al que se une, y a continuación el símbolo de este elemento (X). Se nombran con el nombre del elemento seguido del sufijo "uro", seguidamente, se indica el hidrógeno.
Hidroácidos
Los hidroácidos son las sustancias ácidas que se forman por la unión del hidrógeno con los elementos no metálicos. Se escribe primero el hidrógeno y después el elemento no metálico. Estos compuestos en agua dan disoluciones de carácter ácido y se conocen como ácidos hidroácidos y, así, por ejemplo, se nombran como:
HF, ácido fluorhídrico. H2S, ácido sulfhídrico.
HIDROÁCIDOS.
Son combinaciones de átomos H con átomos de Halógenos (F, Cl, Br, I) o Calcógenos (S, Se, Te), los que actúan con valencia 1 y 2 respectivamente. Son compuestos moleculares gaseosos y su carácter ácido lo manifiestan cuando se disuelven en agua, dando soluciones ácidas.
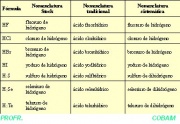
NOMENCLATURA TRADICIONAL:
Nombre genérico: Acido
Nombre específico: sufijo -hídrico a la raíz del nombre del elemento no metálico.
HF ácido fluorhídrico
HCl ácido clorhídrico
HBr ácido bromhídrico
HI ácido yodhídrico
H2S ácido sulfhídrico
H2Se ácido selenhídrico
H2Te ácido telurhídrico
NOMENCLATURA SISTEMÁTICA O STOCK:
Se nombran, agregando el sufijo -uro a la raíz del nombre del elemento no metálico, seguido de la preposición de y de la palabra hidrógeno.
HF fluoruro de hidrógeno
HCl cloruro de hidrógeno
Bibliografia
Información: Garrido, Mª Jesús(2013). Práctica de Compuesto del hidrógeno.Consultado el 11 de marzo del 2014.
Link: https://docs.google.com/file/d/0B1DLmCdkVW6rRmFXR29Ca01MS00/edit?pli=1